Železo a další kovy. Železo, ruthenium a osmium Výskyt v přírodě a výroba Výskyt- nejběžnější nerosty Fe hematit (krevel) Fe 2 O 3, magnetit (magnetovec)Fe. - ppt stáhnout

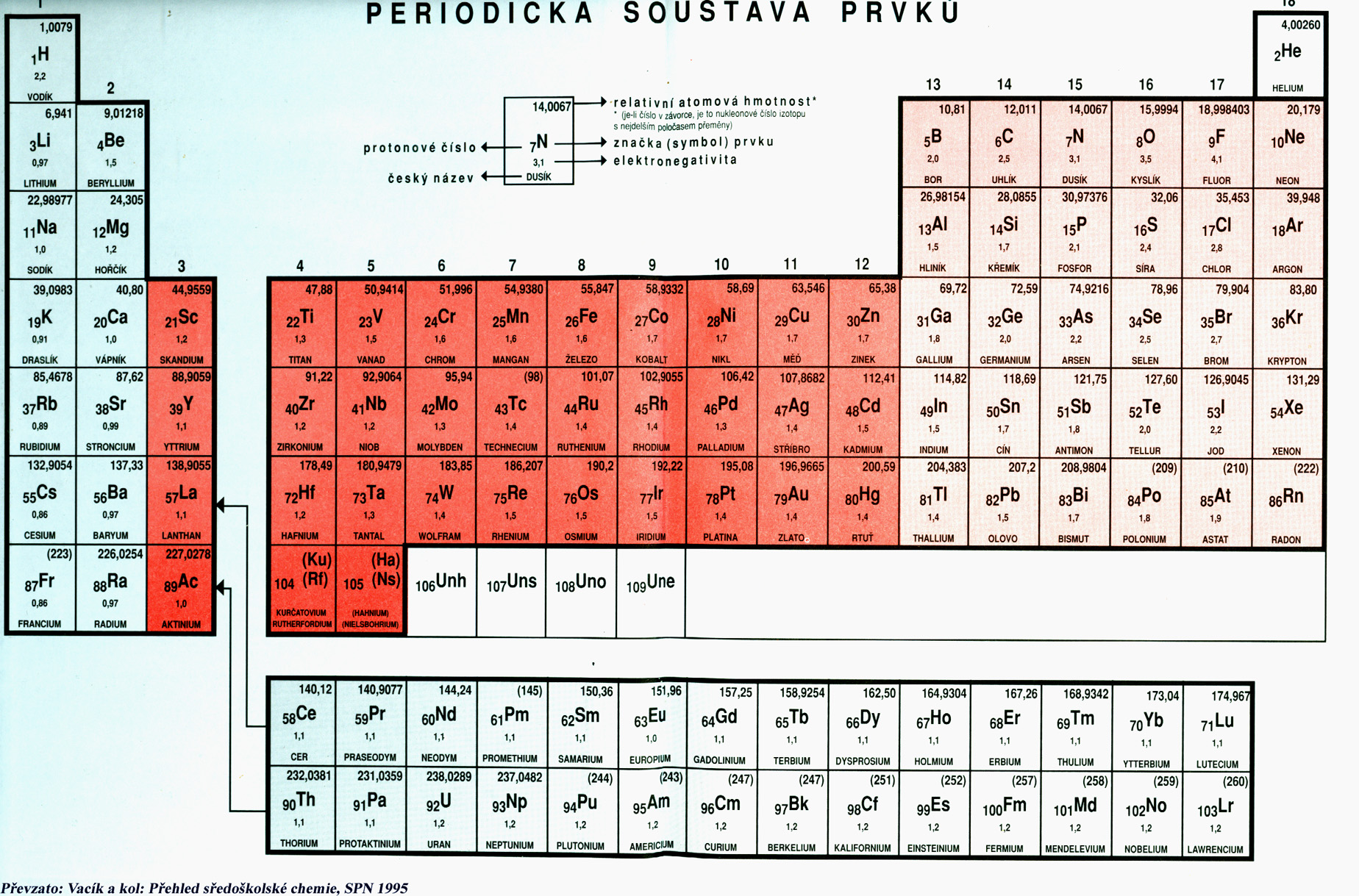
Oxidační číslo je rovno náboji, který by atom získal po p idělení všech vazebných elektronových párů atomům s větší elektronegativitou. - PDF Free Download
Další skupinou anorganických sloučenin jsou oxidy. Oxidy jsou dvouprvkové sloučeniny kyslíku s jiným prvkem. Patří me

Oxidační číslo Volné atomy a atomy v molekulách prvků mají oxidační číslo 0 Oxidační číslo vodíku je ve většině sloučenin rovno +I. Výjimkou jsou sloučeniny. - ppt stáhnout

Oxidační číslo Volné atomy a atomy v molekulách prvků mají oxidační číslo 0 Oxidační číslo vodíku je ve většině sloučenin rovno +I. Výjimkou jsou sloučeniny. - ppt stáhnout

Oxidační číslo Volné atomy a atomy v molekulách prvků mají oxidační číslo 0 Oxidační číslo vodíku je ve většině sloučenin rovno +I. Výjimkou jsou sloučeniny. - ppt stáhnout
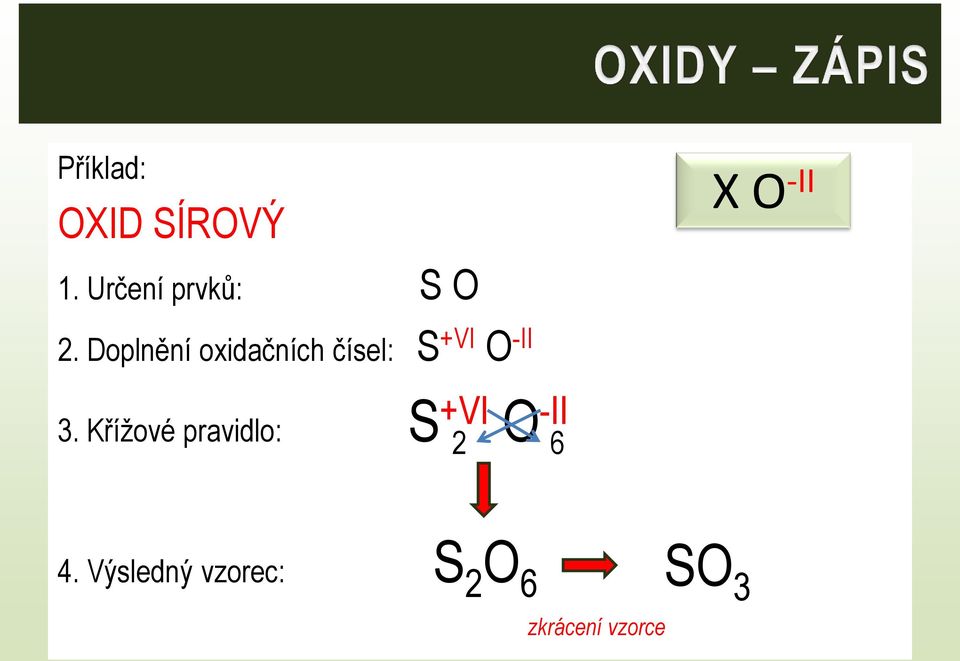
Oxidační číslo je rovno náboji, který by atom získal po p idělení všech vazebných elektronových párů atomům s větší elektronegativitou. - PDF Free Download